古典力学原子モデルを図1-1に示します。図1-1は単純化のため、水素原子モデルを示します。
原子核には+の電荷を持った陽子が1個あり、原子核の回りを-の電荷を持った電子1個が回っています。
以上、古典モデルではエネルギーは任意の連続値をとることができる。
しかし、上記のモデルでは、数々の原子の持つ特性を明確に説明することは困難であり、実用性はありません。
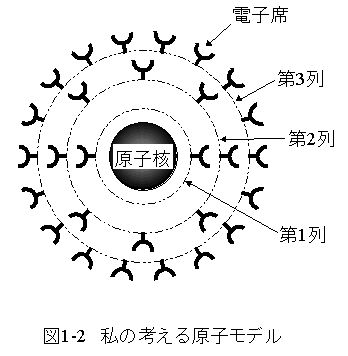
私の考える原子モデル概念図を図1-2に示します。
このモデルは電子配置の概念をベースとしています。
電子配置の詳細については
このモデルは電子配置の概念理解を容易にするため、仮想物体である電子席(電子受容体)を追加しています。
電子席はあくまでも電子配置の可視化のための仮想物体であり、現実の物ではありません。
電子席は離散的エネルギー順位と原子の結合間距離の関係を説明するために付加した概念であり、以下に説明する性質をもちます。
(1)第1列には1sの電子席が2個あります。
(2)第2列には2sの電子席が2個、2pの電子席が6個あります。
(3)第3列には3sの電子席が2個、3pの電子席が6個、3dの電子席が10個あります。
(4)第4列には4sの電子席が2個、4pの電子席が6個、4dの電子席が10個、4fの電子席が14個あります。
(5)同一列の電子席は原子核から等距離にあり同一の「ポテンシャルエネルギー」を持ちます。
(6)s、p、d、fはそれぞれ異なる「運動エネルギー」を持ちます。
(7)電子席の「総エネルギー」は「ポテンシャルエネルギー」+「運動エネルギー」となります。
(8)電子席の「総エネルギー」の低い順は1s→2s→2p→3s→3p→4s→3d→4p→5s→4d→5p→6s→4f→となります。
(9)電子は電子席の「総エネルギー」の低い順に埋まっていきます。
(10)電子は電子席の空いていないところに移動できません。従って電子のエネルギーは連続的では無く不連続に変化します。
(11)電子席は原子核のプラス電荷が作用します。
(12)電子席と電子の間には引力が作用します。
(13)電子席と電子席の間には反発力が作用します。
(14)電子と電子には反発力が作用します。
(15)総合的には電子席、電子間の引力と反発力がバランスする位置に安定すると思われます。
(16)電子席の運動エネルギーはスピン運動と思われます。
(17)電荷がスピン運動しますと磁力が発生しますが、特殊な場合を除き磁力の総和がゼロになるようにスピン運動の回転軸が配置されます。
以上の性質は原子の持つ特性を視覚化して説明するための仮定であり、その有効性は以下の説明でしだいに明らかとなります。
表1-1 主な元素の電子席と電子数
| 電子席 | 第1列 | 第2列 | 第3列 | 第4列 | ||||
| ポテンシャル順位 | 1 | 2 | 2 | 3 | 3 | 3 | 4 | 4 |
| 運動量順位 | l=0 | l=0 | l=1 | l=0 | l=1 | l=2 | l=0 | l=1 |
| 全エネルギー順位 | 1 | 2 | 3 | 4 | 5 | 7 | 6 | 8 |
| 受容電子数 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 6 |
| 電子席固有名称 | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p |
| 原子番号、名称 | 電子数 | 電子数 | 電子数 | 電子数 | 電子数 | 電子数 | 電子数 | 電子数 |
| 1,H,水素 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 2,He,ヘリウム | 2 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 5,B,ホウ素 | 2 | 2 | 1 | 0 | 0 | 0 | 0 | 0 |
| 6,C,炭素 | 2 | 2 | 2 | 0 | 0 | 0 | 0 | 0 |
| 7,N,窒素 | 2 | 2 | 3 | 0 | 0 | 0 | 0 | 0 |
| 8,O,酸素 | 2 | 2 | 4 | 0 | 0 | 0 | 0 | 0 |
| 11,Na,ナトリュウム | 2 | 2 | 6 | 1 | 0 | 0 | 0 | 0 |
| 13,Al,アルミニュウム | 2 | 2 | 6 | 2 | 1 | 0 | 0 | 0 |
| 14,Si,シリコン | 2 | 2 | 6 | 2 | 2 | 0 | 0 | 0 |
| 15,P,リン | 2 | 2 | 6 | 2 | 3 | 0 | 0 | 0 |
| 17,Cl,塩素 | 2 | 2 | 6 | 2 | 5 | 0 | 0 | 0 |
| 24,Cr,クロム | 2 | 2 | 6 | 2 | 6 | 4 | 2 | 0 |
| 26,Fe,鉄 | 2 | 2 | 6 | 2 | 6 | 6 | 2 | 0 |
| 29,Cu,銅 | 2 | 2 | 6 | 2 | 6 | 9 | 2 | 0 |
| 31,Ga,ガリウム | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 1 |
| 32,Ge,ゲルマニュウム | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 2 |
| 33,As,砒素 | 2 | 2 | 6 | 2 | 6 | 10 | 2 | 3 |