燃料電池とは、燃料から直接電気を発電する技術です。ただし、発電とともに発熱もしますので家庭用温水器と組み合わせると省エネルギーに有効です。
燃料電池とは発電機と同様に燃料(水素、酸素)を入力し、直接反応させることで電気エネルギーを出力する、エネルギー変換装置(発電機)です。
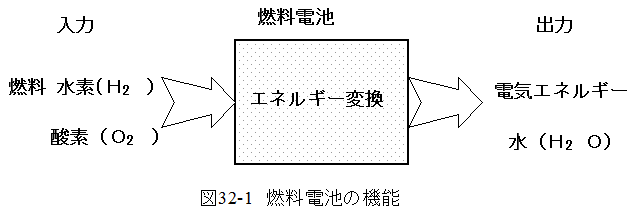
燃料(水素分子)は触媒によりアノード電極部分で水素イオンと電子に分離され、水素イオンは電解質膜を通過し、カソード電極で酸素と結合し水となる。 その際に両電極から外部回路にて経由する電子を電力として使用する。
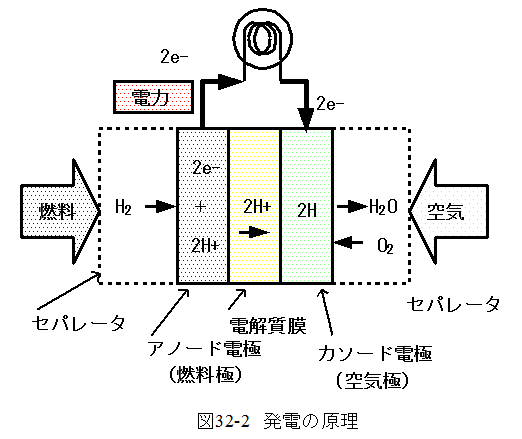
燃料電池の種類を表32-1に示します。
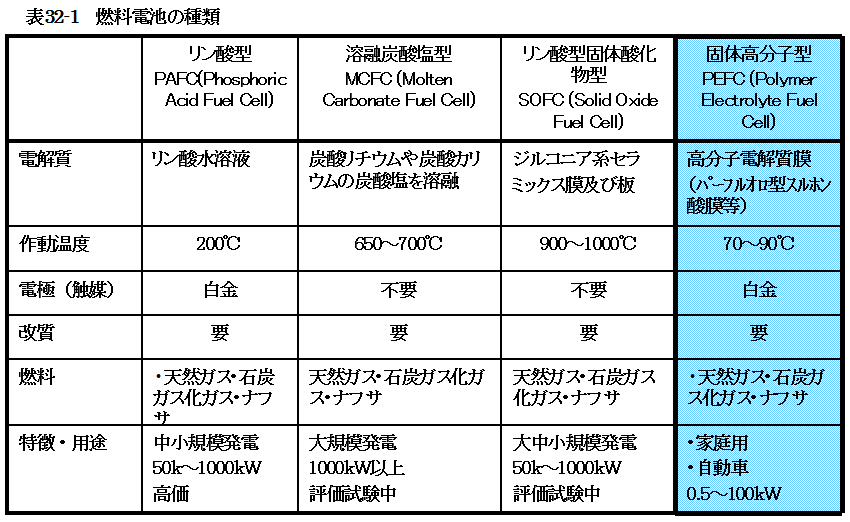
図32-3に固体高分子型燃料電池の基本構造を示します。
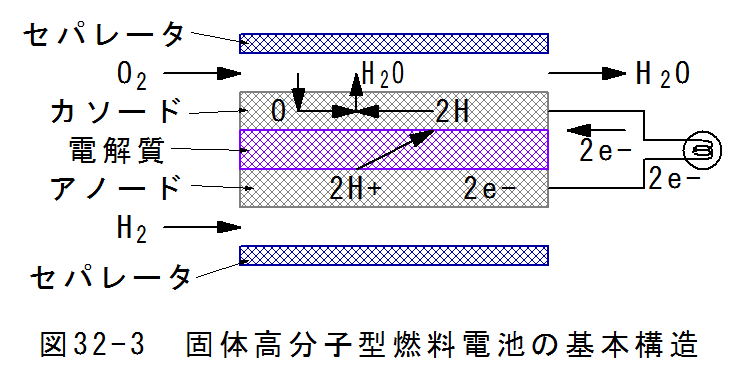
図32-3からわかるように固体高分子型燃料電池の構造はシンプルです。
- セパレータ
セパレータは水素ガスまたは酸素ガスを導く細い溝が設けられています。また酸素側では、水蒸気(H2O)が溝を通して排出されます。
セパレータは絶縁体である必要があります。
- アノードとカソード
アノードがマイナス電極、カソードがプラス電極です。アノードとカソードは導電性の材料である必要があります。低温で反応を起こすには触媒が必要です。触媒とし ては白金(Pt)が優れています。白金(Pt)は高価な材料であり、超微粒子状にして、電極表面に固着させる必要があります。
いかに白金(Pt)の使用量を減らすかが、コスト的に重要となります。
- 電解質
酸素ガスと水素ガスを分離する必要があります。ただし、プラス水素イオンだけを通す必要があります。このため、パーフルオロスルホン酸系ポリマ膜を使用する必要があります。
パーフルオロスルホン酸系ポリマ膜としては、商品名「ナフィオン」(デュポン)が有名です。パーフルオロスルホン酸系ポリマ膜は、プラス水素イオンだけを通す性質があります。
- カソード(プラス電極)での反応
パーフルオロスルホン酸系ポリマ膜はプラス水素イオンを含んでいます。酸素ガスは白金(Pt)の触媒作用により共有結合が破壊され、酸素ラジカルとなります。
プラス水素イオンと酸素ラジカルが反応するためには電子が必要となります。電極は自由電子を豊富にもっていますので、電極から電子2個を奪って反応しH2Oに変化します。また 、この時反応熱が発生し、H2Oは水蒸気となります。
電極は電子を奪われるため、プラスに帯電することになります。
- アノード(マイナス電極)での反応
水素ガスは白金(Pt)の触媒作用により共有結合が破壊され、水素ラジカルとなります。
カソード(プラス電極)側でプラス水素イオンが消費され、電解質はマイナスに帯電します。また、電極は電子が奪われるためプラスに帯電します。
このため、水素ラジカルは電子を放出してプラス水素イオンに変化します。放出された電子はアノード(マイナス電極)側からカソード(プラス電極)側にながれます。
プラス水素イオンは電解質を通してカソード(プラス電極)側に流れます。
- 総合反応
水素ガスと酸素ガスはH2Oに変化します。また、電子がアノード(マイナス電極)側からカソード(プラス電極)側に流れます。(これが発電です。)また、反応熱が発生しま す。(これが発熱です。)
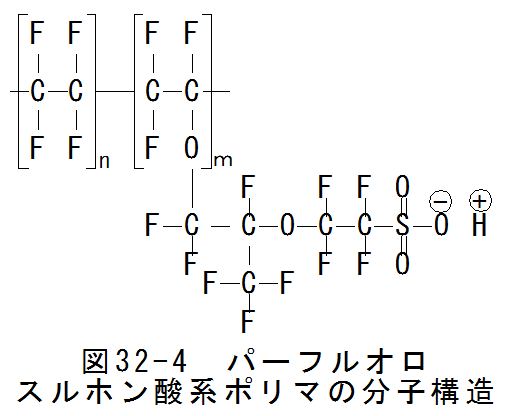
パーフルオロスルホン酸系ポリマの分子構造を図32-4に示します。
図32-4からわかるようにマイナスイオンのスルホン酸はパーフルオロ高分子に結合した構造をしています。
この構造は、イオン交換膜と同じ分子構造であり、マイナスイオンを反発し、プラスイオンを引き付ける特性があります。
パーフルオロスルホン酸系ポリマは水素ガスと酸素ガスを分離し、プラス水素イオンのみを透過する性質があります。
また、母体となる高分子はテフロンと同じであり、耐熱性があり、化学的に安定な材料です。